Informationen und Indikationen für die Praxis
Zystische Tumore
des Pankreas
Tumore der Bauchspeicheldrüse (Pankreas) gehen mit unspezifischen klinischen Symptomen (Ikterus, Fettstühlen, Oberbauchschmerzen, spontan auftretendem Diabetes mellitus) einher oder sind asymptomatisch und werden als Zufallsbefunde diagnostiziert. Neben den soliden Tumoren z. B. dem häufigem duktalem Adenokarzinom werden zystische Tumore des Pankreas unterschieden.
Intraduktale papilläre muzinöse Neoplasie (IPMN)
Die IPMN ist eine prämaligne zystische Erkrankung der 6. – 7. Lebensdekade, die Haupt- und Seitengänge des Pankreasgangsystems betreffen kann 1). Der Hauptgangstyp manifestiert sich bevorzugt im Caput wohingegen der Seitenasttyp neben der Lokalisation im Processus uncinatus in 30 % multifokal auftritt. Daneben existiert auch ein gemischter Typ. Die MRCP kann eine typische Verbindung zum Gangsystem nachweisen. Der Hauptgangstyp zeigt ein höheres Entartungsrisiko. Als Malignitätskriterien gelten murale Knoten, Verkalkungen, eine Zystengröße > 3 cm und eine Gangerweiterung > 10 mm, die in der MRCP / MRT quantifiziert werden können. Es sollten daher zur Risikoquantifizierung initial engmaschige Kontrollen zum Ausschluss einer malignen Entartung erfolgen (3 – 6 Monatsintervall) mit Ausdehnung der Kontrollintervalle im Verlauf. Aus IPMN-Adenomen können sich invasive Pankreaskarzinome entwickeln 2).
Mucinöses Zystadenom (MZN)
Das mucinöse Zystadenom (MZN) des Pankreas ist eine Erkrankung des mittleren Lebensalters (Altersgipfel 47 Jahre), das nahezu ausschließlich Frauen betrifft 3). Das MCN wird als prämaligne bis maligne Läsion eingestuft und geht gewöhnlich mit einer unspezifischen Tumormarkererhöhung von CEA und CA 19 – 9 einher (Ovar-ähnliches Stroma). 80 % treten im Pankreasschwanz / ‑corpus auf und 20 % im Bereich des Pankreaskopfes 4). Morphologisch imponiert das mucinöse Zystadenom als rundlich-ovaler, makrozystischer oder unilobulärer Tumor mit heterogenem Kontrastmittelenhancement teils mit linearen/kurvenlinearen Binnensepten und möglichen Randverkalkungen (Radiopaedia 2017). Das Bild entspricht einer «Orangenschnittfläche» bzw. «Zysten in Zyste» mit glatter Außenkontur 1). Der Malignomverdacht wird bei muralen Knoten in der Zystenwand, einer Zystengröße > 6 cm und peripheren Eierschalenverkalkungen erhärtet.
Pancreaspseudozysten
Pankreaspseudozysten gehören zu den häufigsten zystischen Veränderungen des Pankreas. Sie treten im Rahmen akuter oder chronischer Pankreatiden auf. Pseudozysten sind flüssige Kollektionen die im Rahmen einer schweren inflammtorischen Reaktion nach ca. 4 – 6 Wochen eine Kapsel bzw. fibrotisches Gewebe ausbilden können (Atlantaklassifikation 2012, 5)). Pathophysiologisch entstehen sie durch eine Leckage von digestiven Pankreasenzymen aus dem Pankreasgangsystem, wobei in ca. 50 % eine Kommunikation mit dem Pankresgangsystem erhalten bleibt 6). Die Pseudozysten finden sich häufig in der Pankreasloge – können aber auch variabel von der Leiste bis hin zum Mediastinum auftreten 7). Als Komplikationen können sekundäre Infektionen und durch den raumfordernden Charakter eine biläre Obstruktion, Hydronephrose, Magenausgangsobstruktion etc. auftreten. In der MRT imponieren die typischen Pankreaspseudozysten somit als rundlich-ovale flüssigkeitsisointense (T2-hyperintense / T1-hypointense) Läsionen mit einer kapsulären Begrenzung, die ein mittleres frühes Enhancement mit Progress über die Zeit aufzeigen 8) 5). Durch die MRT kann insbesondere eine spezifische Schichtbildung bei «Zelltrümmern» innerhalb der Pankreaszysten in der T2-Wichtung nachgewiesen werden 9). Zysten mit einer Größe < 4 – 6 cm zeigen häufig eine Spontanremission. Bei stark raumforderndem Charakter oder Sekundärinfektion kann eine chirurgische Sanierung notwendig werden.
Pankreaszysten
Einfache Pankreaszysten treten bei Syndromen/Erkrankungen wie z. B. Hippel-Lindau-Syndrom, zystischer Fibrose oder autosomal-dominanter polyzystischer Nierenerkrankung gehäuft auf.
Serös zystische Neoplasie (SZN)
Die serös zystisch Neoplasie ist eine oligozystische oder polyzystische Erkrankung des Pankreas, die überwiegend Frauen (F:M 4:1) mit einer Altersverteilung > 60 Jahren betrifft. Die oligozystische Form imponiert mit Makrozysten (Zysten > 2 cm) oder unilobulär bevorzugt im Pankreaskopfbereich. Die mikrozystische Form zeigt multiple (n > 6) „traubenartig“ konfigurierte Zystenkonglomerate (Zysten < 1 cm) mit möglicher Lokalisation im gesamten Pankreas – teils mit charakterisierender zentraler verkalkender Narbe in 30 % 1). Die Zysten imponieren im MRT flüssigkeitsisointens (T2-hyperintens / T1–hypointens), wohingegen die Narbe T2-hypointens imponiert und aufgrund des fibrösen Charakters in der Spätphase ein Kontrastmittelenhancement aufzeigt. Es besteht keine Ganganbindung an den Ductus pancreaticus. Die Läsionen zeigen in weniger als 3 % eine maligne Entartung (97 % benigne) 2).
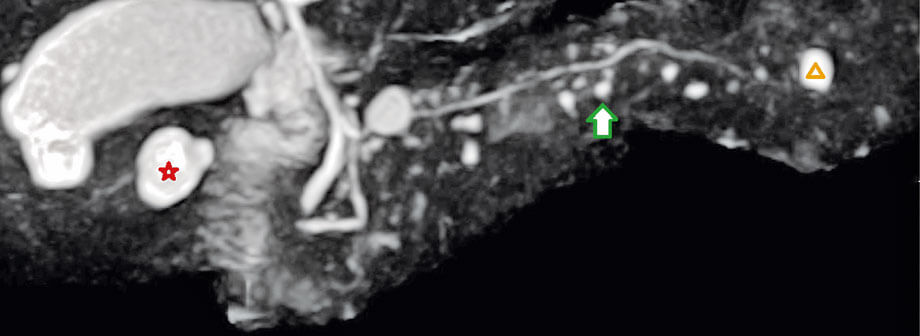
Abbildung: IPMN des Pankreas vom Seitenasttyp (Pfeil) / Pankreasschwanzzyste (Dreieck) / Leberzyste (Stern) in der MRCP
Literatur / Quellen:
1: Buerke B et al. (2010). Differential diagnosis and radiological management of cystic pancreatic lesions. Rofo; 182: 852 – 860. | 2: Kalb B et al. (2009). MR imaging of cystic lesions of the pancreas. Radiographics; 29(6): 1749 – 1765. | 3: Lee WA (2005). Mucinous cystadenoma of the pancreas with predominant stroma creating a solid tumor. World J Surg Oncol.; 3: 59. | 4: Gore RM et al. (2012). The incidental cystic pancreas mass: a practical approach. Cancer Imaging. 2012; 12(2): 414 – 421. | 5: Thoeni RF (2012). The revised Atlanta classification of acute pancreatitis: its importance for the radiologist and its effect on treatment. Radiology.; 262(3): 751 – 764. | 6: Lucey BC & Kuligowska E (2006). Radiologic management of cysts in the abdomen and pelvis. AJR Am J Roentgenol.; 186(2): 562 – 573. | 7: Karantanas AH et al (2003). Extension of pancreatic pseudocysts into the neck: CT and MR imaging findings. AJR Am J Roentgenol.;180(3): 843 – 845. | 8: Semelka RC (2006). Abdominal-pelvic MRI. Wiley. (2006) ISBN:0471692735. | 9: Macari M et. al. (2009). Differentiating pancreatic cystic neoplasms from pancreatic pseudocysts at MR imaging: value of perceived internal debris. Radiology.; 251(1): 77 – 84.